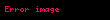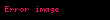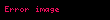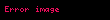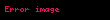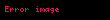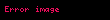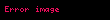İzobar proses (yun. "baros" – ağırlıq, çəki) – makroskopik sistemin halının sabit təzyiqdə dəyişməsi prosesi (p = const). Qazı qızdırdıqda onun hərəkət edən porşenli silindrdə genişlənməsini izobar proses hesab etmək olar. İzobar prosesi aşağıdakı nisbətlərə bərabərdir:
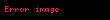
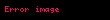
Sistemə ötürülən istilik enerjisi iş görülməsinə və sistemin daxili enerjisinin (U) dəyişməsinə sərf olunur. Termodinamikanın birinci qanununa əsasən
burada W qaz tərəfindən görülən iş, U qazın daxili enerji və Q verilən istilik enerjisidir. Qapalı sistemdə təzyiq-həcm işi aşağıdakı kimi müəyyən edilir:
burada Δ bütün proses üzrə dəyişiklik deməkdir, d isə diferensialı bildirir. Təzyiq sabit olduğundan, bu o deməkdir ki
İdeal qaz qanununu tətbiq etməklə, alırıq ki
R qaz sabitini, n isə sabit qaldığını qəbul etdiyimiz maddənin miqdarını ifadə edir (məsələn, kimyəvi reaksiya zamanı faza keçidi yoxdur).Daxili enerjinin dəyişməsi sistemin temperaturundan asılıdır.
burada cV,m sabit həcmdə molar istilik tutumudur.
Son iki tənliyi birinci tənliylə əvəz etməklə izobar qazlar üçün verilən istiliyin təsiri altında qazın temperatur dəyişməsini təyin edə bilərik.
burada cP sabit təzyiqdə molar istilik tutumudur.
İstinadlar
- Peter Olver (1999), Classical Invariant Theory, p. 217
Xarici keçidlər
- Veranschaulichung der Zustandsänderungen mit kleinen interaktiven Animationen Arxivləşdirilib 2011-08-26 at the Wayback Machine
- Die allgemeine Gasgleichung mit Diagrammen und interaktiver Animation
wikipedia, oxu, kitab, kitabxana, axtar, tap, meqaleler, kitablar, oyrenmek, wiki, bilgi, tarix, tarixi, endir, indir, yukle, izlə, izle, mobil, telefon ucun, azeri, azəri, azerbaycanca, azərbaycanca, sayt, yüklə, pulsuz, pulsuz yüklə, haqqında, haqqinda, məlumat, melumat, mp3, video, mp4, 3gp, jpg, jpeg, gif, png, şəkil, muisiqi, mahnı, kino, film, kitab, oyun, oyunlar, android, ios, apple, samsung, iphone, pc, xiomi, xiaomi, redmi, honor, oppo, nokia, sonya, mi, web, computer, komputer
Izobar proses yun baros agirliq ceki makroskopik sistemin halinin sabit tezyiqde deyismesi prosesi p const Qazi qizdirdiqda onun hereket eden porsenli silindrde genislenmesini izobar proses hesab etmek olar 1 Izobar prosesi asagidaki nisbetlere beraberdir Izobar proses V T c o n s t displaystyle V over T const V 2 V 1 T 2 T 1 displaystyle V 2 over V 1 T 2 over T 1 Sari sahe gorulen isi eks etdirir Sisteme oturulen istilik enerjisi is gorulmesine ve sistemin daxili enerjisinin U deyismesine serf olunur Termodinamikanin birinci qanununa esasen Q D U W displaystyle Q Delta U W burada W qaz terefinden gorulen is U qazin daxili enerji ve Q verilen istilik enerjisidir Qapali sistemde tezyiq hecm isi asagidaki kimi mueyyen edilir W p d V displaystyle W int p dV burada D butun proses uzre deyisiklik demekdir d ise diferensiali bildirir Tezyiq sabit oldugundan bu o demekdir ki W p D V displaystyle W p Delta V Ideal qaz qanununu tetbiq etmekle aliriq ki W n R D T displaystyle W n R Delta T R qaz sabitini n ise sabit qaldigini qebul etdiyimiz maddenin miqdarini ifade edir meselen kimyevi reaksiya zamani faza kecidi yoxdur Daxili enerjinin deyismesi sistemin temperaturundan asilidir D U n c V m D T displaystyle Delta U n c V m Delta T burada cV m sabit hecmde molar istilik tutumudur Son iki tenliyi birinci tenliyle evez etmekle izobar qazlar ucun verilen istiliyin tesiri altinda qazin temperatur deyismesini teyin ede bilerik Q n c V m D T n R D T Q n D T c V m R Q n D T c P m displaystyle begin aligned Q amp n c V m Delta T n R Delta T Q amp n Delta T c V m R Q amp n Delta Tc P m end aligned burada cP sabit tezyiqde molar istilik tutumudur Istinadlarredakte Peter Olver 1999 Classical Invariant Theory p 217Xarici kecidlerredakte nbsp Vikianbarda Izobar proses ile elaqeli mediafayllar var Veranschaulichung der Zustandsanderungen mit kleinen interaktiven Animationen Arxivlesdirilib 2011 08 26 at the Wayback Machine Die allgemeine Gasgleichung mit Diagrammen und interaktiver Animation Menbe https az wikipedia org w index php title Izobar proses amp oldid 8045483
 Azərbaycanca
Azərbaycanca Deutsch
Deutsch Lietuvos
Lietuvos සිංහල
සිංහල Türkçe
Türkçe Українська
Українська