| Kadmium xlorid | |
|---|---|
 | |
 | |
| Ümumi | |
| Kimyəvi formulu | CdCl2 |
| Fiziki xassələri | |
| Molyar kütlə | 183,32 q/mol |
| Sıxlıq | 4,047 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 564; 568,5 °C |
| Qaynama nöqtəsi | 960 °C |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 10108-64-2 |
| PubChem | 24947, 24633 |
| 233-296-7 | |
| SMILES |
|
| |
| RTECS | EV0175000 |
| ChEBI | 35456 |
| BMT nömrəsi | 2570 |
| ChemSpider | 23035 |
| Məlumatlar (25 °C, 100 kPa) üçün verilmişdir. | |
Kadmium (II) xlorid (CdCl2) — qeyri-üzvi bir birləşmədir, kadmium metalının və xlorid turşusunun duzu, rəngsizkristallar, higroskopik, suda asanlıqla həll olunur, kristallohidratlar əmələ gətirir.
Fiziki xassələri
| ]Kadmium (II) xlorid heksoqonal sistemin rəngsiz kristallarını, fəza qrupunu R-3m, hüceyrə parametrlərini a = 0.385 nm, c = 1.746 nm, Z = 3 əmələ gətirir. Sulu məhlulları hidrolizə görə turş reaksiya yaradır. Metalik kadmium(6000C-də kadmiumun~ 15%) kadmium xloridin ərintisində həll olunur.
Alınması
| ]Metalik kadmiumun xlorid turşusunda həll edilməsi nəticəsində almaq olur:
Kadmium oksidin xlorid turşusunda həll edilməsi:
Sadə maddələr arasındakı reaksiya nəticəsində:
Kadmium oksidin və xlor qazı ilə reaksiyası nəticəsində:
Kimyəvi xassələri
| ]Kristallohidratların qızdırılması nəticəsində susuz duzları alınır:
Hidrogen xloridlə və qələvi metal xloridlərlə kompleks yaradır:
Qaynar qatı sulfat turşusu ilə reaksiyaya daxil olur:
Qələvilərlə reksiyaya daxil olur:
Tədqiqi
| ]Fotoreagentlərdə. Qalvanik elementlərdə elektrolitin tərkib hissəsi kimi. Üzvi sintezdə katalizator kimi. Sənayedə günəş panellərinin istehzalı zamanı.
İstinadlar
| ]- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.-Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с
- David R. Lide, Jr. Basic laboratory and industrial chemicals (ing.): A CRC quick reference handbook. CRC Press, 1993.
wikipedia, oxu, kitab, kitabxana, axtar, tap, meqaleler, kitablar, oyrenmek, wiki, bilgi, tarix, tarixi, endir, indir, yukle, izlə, izle, mobil, telefon ucun, azeri, azəri, azerbaycanca, azərbaycanca, sayt, yüklə, pulsuz, pulsuz yüklə, haqqında, haqqinda, məlumat, melumat, mp3, video, mp4, 3gp, jpg, jpeg, gif, png, şəkil, muisiqi, mahnı, kino, film, kitab, oyun, oyunlar, android, ios, apple, samsung, iphone, pc, xiomi, xiaomi, redmi, honor, oppo, nokia, sonya, mi, web, computer, komputer
Vikipediya azad ensiklopediya Kadmium xloridUmumiKimyevi formulu CdCl2Fiziki xasseleriMolyar kutle 183 32 q molSixliq 4 047 q sm Termik xususiyyetlerErime noqtesi 564 568 5 CQaynama noqtesi 960 CTesnifatiCAS da qeyd nom 10108 64 2PubChem 24947 24633233 296 7SMILES Cl Cd Cl InChI 1S Cd 2ClH h 2 1H q 2 p 2YKYOUMDCQGMQQO UHFFFAOYSA LRTECS EV0175000ChEBI 35456BMT nomresi 2570ChemSpider 23035Melumatlar 25 C 100 kPa ucun verilmisdir Kadmium II xlorid CdCl2 qeyri uzvi bir birlesmedir kadmium metalinin ve xlorid tursusunun duzu rengsizkristallar higroskopik suda asanliqla hell olunur kristallohidratlar emele getirir Fiziki xasseleri span Kadmium II xlorid heksoqonal sistemin rengsiz kristallarini feza qrupunu R 3m huceyre parametrlerini a 0 385 nm c 1 746 nm Z 3 emele getirir Sulu mehlullari hidrolize gore turs reaksiya yaradir Metalik kadmium 6000C de kadmiumun 15 kadmium xloridin erintisinde hell olunur Alinmasi span Metalik kadmiumun xlorid tursusunda hell edilmesi neticesinde almaq olur Cd 2HCl t CdCl2 H2 displaystyle mathsf Cd 2HCl xrightarrow tau CdCl 2 H 2 uparrow dd Kadmium oksidin xlorid tursusunda hell edilmesi CdO 2HCl CdCl2 H2O displaystyle mathsf CdO 2HCl xrightarrow CdCl 2 H 2 O dd Sade maddeler arasindaki reaksiya neticesinde Cd Cl2 450 500oC CdCl2 displaystyle mathsf Cd Cl 2 xrightarrow 450 500 o C CdCl 2 dd Kadmium oksidin ve xlor qazi ile reaksiyasi neticesinde 2CdO 2Cl2 500 600oC 2CdCl2 O2 displaystyle mathsf 2CdO 2Cl 2 xrightarrow 500 600 o C 2CdCl 2 O 2 dd Kimyevi xasseleri span Kristallohidratlarin qizdirilmasi neticesinde susuz duzlari alinir CdCl2 2 5H2O 120 170oC CdCl2 2 5H2O displaystyle mathsf CdCl 2 cdot 2 5H 2 O xrightarrow 120 170 o C CdCl 2 2 5H 2 O dd Hidrogen xloridle ve qelevi metal xloridlerle kompleks yaradir CdCl2 2HCl H2 CdCl4 displaystyle mathsf CdCl 2 2HCl xrightarrow H 2 CdCl 4 CdCl2 2KCl K2 CdCl4 displaystyle mathsf CdCl 2 2KCl xrightarrow K 2 CdCl 4 downarrow dd Qaynar qati sulfat tursusu ile reaksiyaya daxil olur CdCl2 H2SO4 100oC CdSO4 2HCl displaystyle mathsf CdCl 2 H 2 SO 4 xrightarrow 100 o C CdSO 4 2HCl uparrow dd Qelevilerle reksiyaya daxil olur CdCl2 2NaOH Cd OH 2 2NaCl displaystyle mathsf CdCl 2 2NaOH xrightarrow Cd OH 2 2NaCl dd Tedqiqi span Fotoreagentlerde Qalvanik elementlerde elektrolitin terkib hissesi kimi Uzvi sintezde katalizator kimi Senayede gunes panellerinin istehzali zamani Istinadlar span Spravochnik himika Redkol Nikolskij B P i dr 2 e izd ispr M L Himiya 1966 T 1 1072 s Spravochnik himika Redkol Nikolskij B P i dr 3 e izd ispr L Himiya 1971 T 2 1168 s Lidin R A i dr Himicheskie svojstva neorganicheskih veshestv Ucheb posobie dlya vuzov 3 e izd ispr M Himiya 2000 480 sDavid R Lide Jr Basic laboratory and industrial chemicals ing A CRC quick reference handbook CRC Press 1993 ISBN 978 0 8493 4498 5 Kateqoriyalar Qeyri uzvi birlesmelerXloridlerGizli kateqoriyalar Vikipediya Vikidatada menbeleri olan meqalelerISBN sehrli kecidlerinin istifade olundugu sehifeler
 Azərbaycanca
Azərbaycanca Deutsch
Deutsch 日本語
日本語 Lietuvos
Lietuvos සිංහල
සිංහල Türkçe
Türkçe Українська
Українська United State
United State
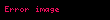
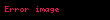
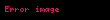
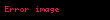
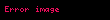
![{\displaystyle {\mathsf {CdCl_{2}+2HCl\ \xrightarrow {} \ H_{2}[CdCl_{4}]}}}](https://www.wikimedia.az-az.nina.az/image/aHR0cHM6Ly93d3cud2lraW1lZGlhLmF6LWF6Lm5pbmEuYXovaW1hZ2UvYUhSMGNITTZMeTkzYVd0cGJXVmthV0V1YjNKbkwyRndhUzl5WlhOMFgzWXhMMjFsWkdsaEwyMWhkR2d2Y21WdVpHVnlMM04yWnk5bFpqTmhZalF5WTJKaE5EQmpZV0V6TkRBelpEUXlaR1k1WXpJeFkyTmlZamsyWmpGa056VTEuc3Zn.svg)
![{\displaystyle {\mathsf {CdCl_{2}+2KCl\ \xrightarrow {} \ K_{2}[CdCl_{4}]\downarrow }}}](https://www.wikimedia.az-az.nina.az/image/aHR0cHM6Ly93d3cud2lraW1lZGlhLmF6LWF6Lm5pbmEuYXovaW1hZ2UvYUhSMGNITTZMeTkzYVd0cGJXVmthV0V1YjNKbkwyRndhUzl5WlhOMFgzWXhMMjFsWkdsaEwyMWhkR2d2Y21WdVpHVnlMM04yWnk4NFlXWXlZamsxWWpneU1UVTVaakV6WldNM05qUmxOVGxpT0RNNFpEWmxZak5sWVRZM01qa3guc3Zn.svg)